Decyzją Głównego Inspektoratu Farmaceutycznego z dnia 22 sierpnia 2019 r. wycofano z obrotu 13 popularnych leków, przepisywanych masowo pacjentom na przeziębienie i grypę.
Fenspiryd bardziej szkodzi niż leczy
Fenspiryd (łac. Fenspiridum) jest stosowany jako substancja czynna działająca przeciwzapalnie w infekcjach górnych dróg oddechowych, ma też silne działanie przeciwuczuleniowe i rozkurczające oskrzela. Lek miał hamować wytwarzanie histaminy oraz serotoniny, a także zmniejszać obrzęki błony śluzowej układu oddechowego. W ulotkach preparatów z fenspirydem można przeczytać, że hamują procesy zapalne oraz nadmierne wydzielanie oskrzelowe. Jednak, jak czytamy w komunikacie GIF, przeprowadzone badania wykazały, że "stosunek korzyści do ryzyka produktów leczniczych zawierających fenspiryd nie jest korzystny".
Masowo przepisywane dzieciom
Leki zawierające fenspiryd były masowo przepisywane małym pacjentom. Niestety, okazało się, że ta substancja czynna niesie dla organizmu więcej zagrożeń niż korzyści terapeutycznych. Te środki mogły prowadzić do zaburzeń żołądkowo-jelitowych, bóli brzucha i nudności, a w niektórych przypadkach także do zaburzeń pracy serca.W serwisach społecznościowych wielu rodziców komentuje, że środki lecznicze z substancją czynną fenspiryd były masowo przepisywane ich dzieciom:
„Pulneo pediatrzy hurtowo wypisywali dzieciom”
„Mój syn (teraz juz 12-letni) wypił tego hektolitry. Za każdym razem lekarz przepisywał a ja się cieszyłam, że udało się bez antybiotyku echhh”
„Zawsze używałam Pulneo”
„Fosidal u nas był często na kaszel”
„Mój syn tak często choruje, że raz na dwa tygodnie wizyta u lekarza kończyła się receptą z wypisanym fosidalem, sporadycznie pulneo...no ale wypił tego takie ilości, że aż strach...”
Potwierdzone podejrzenia
Wycofanie leków z rynku jest konsekwencją decyzji z 11.02.2019 r., gdy Główny Inspektorat Farmaceutyczny wstrzymał 13 leków w związku z podejrzeniami o szkodliwości substancji czynnej zawartej w lekach, tj. fenspirydu. Francuska agencja ds. leków ANSM (Agence nationale de sécurité du médicament et des produits de santé) wnioskowała do Europejskiej Agencji Leków o wszczęcie pilnej procedury unijnej, by ponownie ocenić stosunek korzyści do ryzyka produktów leczniczych z fenspirydem w składzie.Pharmacovigilance Risk Assessment Committee stwierdził, że stosunek korzyści do ryzyka produktów leczniczych zawierających fenspiryd nie jest korzystny. Dlatego 22 sierpnia 2019 roku GIF zadecydował o wycofaniu z obrotu 13 popularnych w Polsce leków na przeziębienie.
„Powodowanie zagrożenia życia lub zdrowia choćby dla jednego, kilku czy jakiejkolwiek innej liczby pacjentów rodzi konieczność nadania niniejszej decyzji rygoru natychmiastowej wykonalności” – czytamy w decyzji GIF z 22.08.2019 r.
Leki wycofane z obrotu przez GIF
Na liście wycofanych z obrotu na terytorium Polski leków znalazły się:
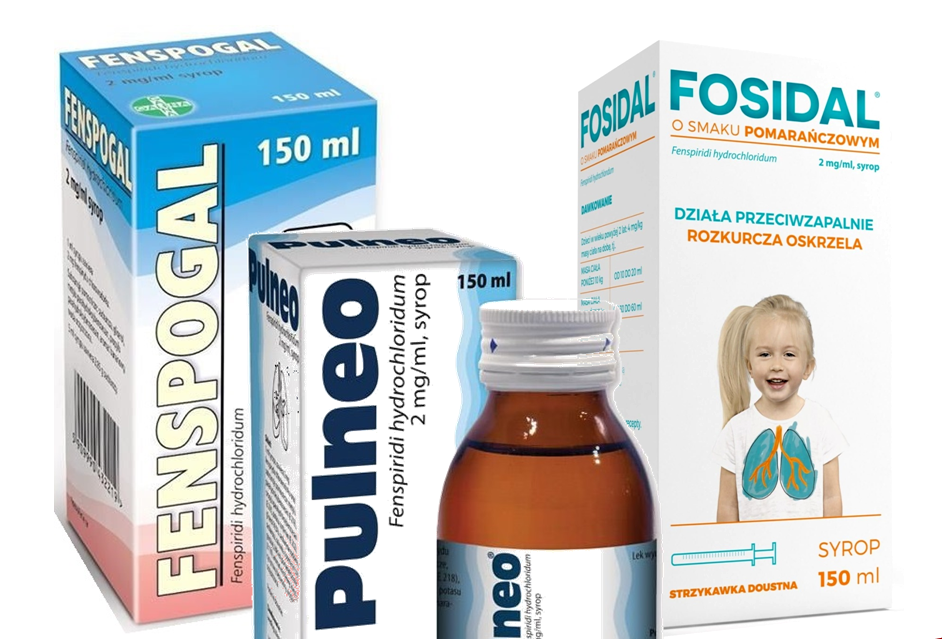
- Pulneo o smaku coli 2mg/ml, podmiot odpowiedzialny Aflofarm Farmacja Polska Sp. z o.o.
- Pulneo 2 mg/ml, podmiot odpowiedzialny Aflofarm Farmacja Polska Sp. z o.o.
- Pulneo 25 mg/ml, podmiot odpowiedzialny Aflofarm Farmacja Polska Sp. z o.o.
- Fosidal o smaku pomarańczowym 2 mg/ml, podmiot odpowiedzialny Medana Pharma S.A.
- Fosidal o smaku malinowym 2 mg/ml, podmiot odpowiedzialny Medana Pharma S.A
- Fenspogal 2 mg/ml, podmiot odpowiedzialny Farmaceutyczna Spółdzielnia Pracy Galena
- Eurespal 80 mg, importowany do Polski przez Laboratorium Galenowe Olsztyn Sp. z o.o
- Eurespal 80 mg, importowany do Polski przez Laboratorium Galenowe Olsztyn Sp. z o.o.
- Eurespal 80 mg, importowany do Polski przez Laboratorium Galenowe Olsztyn Sp. z o.o.
- Eurespal 80 mg, importowany do Polski przez Laboratorium Galenowe Olsztyn Sp. z o.o.
- Eurespal 80 mg, podmiot odpowiedzialny w kraju eksportu Les Laboratoires Servier, importer równoległy Forfarm Sp. z o.o.
- Eurefin 2 mg/ml, podmiot odpowiedzialny Przedsiębiorstwo Produkcji Farmaceutycznej HASCO-LEK S.A.
- Elofen 2 mg/ml, podmiot odpowiedzialny Polfarmex S.A.

Komentarze (0)